Микропенис: причины, диагностика, лечение
Содержание статьи:
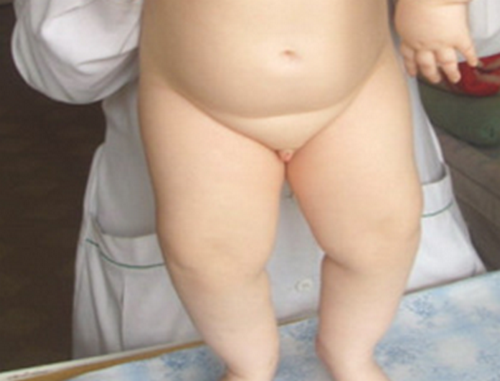
Микропенис – врожденная патология, связанная с дефицитом андрогенов в период внутриутробного развития, уменьшение от нормальной возрастной длины на 2,5 стандартных отклонения. Средняя длина вытянутого пениса у доношенного новорожденного мальчика составляет примерно 3,5 см. Размер органа менее 2-2,5 см требует оценки детского андролога-уролога. Данная патология может сочетаться с другими пороками развития – эписпадией, гипоспадией, неопущением яичек в мошонку, проявляться самостоятельно или быть частью генетического синдрома. Иногда микропенис рассматривают как форму неоднозначных гениталий, но пальпируемые нормальные яички в мошонке указывают на высокую вероятность нормального мужского кариотипа. Если тестикулы не определяются и/или отсутствует мочеиспускательный канал, требуется консультация по поводу нарушений полового развития. Микропенис не следует путать со скрытым половым членом, когда у ребенка, страдающего ожирением, соответствующий всем возрастным нормам половой орган спрятан под толщей жировой складки.
Физиология и патогенез
Производство тестостерона (Т) у плода и его периферическое превращение в дигидротестостерон (ДГТ) необходимо для нормального развития мужчины. В начале беременности плацентарный хорионический гонадотропин человека (ХГЧ) стимулирует развивающиеся яички к выработке Т путем связывания с рецептором лютеинизирующего гормона (ЛГ). Примерно через 14 недель беременности у ребенка активизируется гипоталамо-гипофизарно-гонадная ось, и выработка тестостерона попадает под контроль ЛГ плода. Рост полового члена после первого триместра зависит от выработки гонадотропина плода. Т преобразуется ферментом 5-альфа-редуктазой в более мощный андроген – дигидротестостерон, который отвечает за вирилизацию наружных половых органов мужчины. Интактные периферические андрогенные рецепторы также важны для нормального мужского развития.
После первоначального всплеска лютеинизирующего гормона (ЛГ) и Т при рождении, продолжающегося около 12 часов, уровень гонадотропинов ЛГ, фолликулостимулирующего гормона (ФСГ) и тестостерона низок в течение первых нескольких дней жизни. Приблизительно через неделю уровни гонадотропина и Т начинают подниматься до пубертатных уровней, достигая пика в возрасте 1-3 месяцев, а затем снижаясь к 6 месяцам до препубертатных значений. После полугода жизни небольшой последующий рост полового члена происходит параллельно соматическому росту. С наступлением полового созревания рост пениса возобновляется из-за увеличения выработки Т. Гормон роста также играет роль в росте полового члена, так как микропенис диагностируют у детей с изолированным дефицитом соматотропина.
Микропенис может быть вызван дисфункцией в любом месте вдоль гипоталамо-гипофизарно-гонадной оси, дефектом периферического действия андрогенов, изолированным дефицитом гормона роста, первичной структурной аномалией или является частью генетического синдрома. Наиболее распространенной причиной микропениса является нарушение функции гипоталамуса или гипофиза. Микропенис также может возникать у детей с дефектами рецептора ЛГ или биосинтеза тестостерона (например, дефицит 17-бета-гидроксистероиддегидрогеназы), в этом случае при рождении половые органы будут по женскому типу или неоднозначны. У некоторых мальчиков диагностируют микропению.
Дефекты периферического действия андрогенов включают дефицит 5-альфа-редуктазы и синдром частичной андрогенной нечувствительности из-за дефекта рецептора андрогена. Большинство детей с этими состояниями имеют различную степень неполного лабиоскротального слияния, что приводит к гипоспадии и неоднозначности гениталий. Генетические синдромы, в которых микропенис может быть характерной чертой, включают синдромы Прадера-Вилли, Кляйнфельтера и Нунана.
Причины микропениса
Наиболее часто причинами формирования микропениса являются гипогонадотропный гипогонадизм (поражение гипоталамуса и гипофиза) и гипергонадотропный гипогонадизм (патологический процесс непосредственно в яичках). Условия, связанные с гипогонадотропным гонадизмом:
• Синдром Каллмана (Кальмана)
Аносмия (отсутствие обоняния) или гипосомия является характерной чертой синдрома Каллмана, который встречается у 1 на 10000 мужчин. Основной аномалией является неспособность миграции гонадотропин-рилизинг-гормона (GnRH) и обонятельных нейронов из обонятельной плакоды в их соответствующие местоположения в гипоталамусе и обонятельной луковице, соответственно. Около половины мужчин с синдромом Каллмана рождаются с микропенисом. Тип наследования аутосомно-доминантный (среди прочих, ген FGFR1 / KAL-2 ), аутосомно-рецессивный или Х-сцепленный рецессивный (KAL-1ген). Связанные аномалии могут включать расщелину губы и неба, почечную агенезию, нейросенсорную тугоухость, нарушения зрения, синкинезию (зеркальные движения), мозжечковую атаксию, агенезию мозолистого тела, короткие пястные кости или pes cavus. На МРТ головного мозга у 90% пациентов наблюдаются аномальные или отсутствующие обонятельные луковицы.
• Изолированный гипогонадотропный гипогонадизм
Обоняние не страдает, что играет роль в дифференциации изолированного гипогонадотропного гипогонадизм от синдрома Каллмана. Специалисты полагают, что при синдроме Каллмана наблюдается более высокая склонность к развитию сложного фенотипа, чем при изолированном гипогонадотропном гипогонадизме.
• Множественный дефицит гормонов гипофиза
Часто у пациентов с данной патологией регистрируют гипогликемию, которая возникает на фоне дефицита соматотропина и адренокортикотропного гормона (АКТГ). Гипопитуитаризм может быть вторичным по отношению к мутациям транскрипционных факторов (например, PROP-1, LHX3 ).
• Септооптическая дисплазия (СОД)
Основные признаки СОД включают: отсутствующую перегородочную перепонку, гипоплазию зрительного нерва и гипопитуитаризм, реже - блуждающий нистагм. Дефицит гормонов гипофиза может выявляться при рождении или развиваться годами. Мутации в гене HESX1 ( RPX ) связывают с СОД.
Состояния, связанные со снижением выработки андрогенов и гипергонадотропным гипогонадизмом:
• Анорхия
Исчезающие яички или синдром регрессии яичек подразумевает отсутствие тестикул при нормальном мужском кариотипе. Микропенис формируется, когда дегенерация половых желез происходит после 12-14 недель беременности. Патология потенциально связана с перекрутом или другим сосудисто-окклюзионным явлением в матке.
• Дефекты LH-рецептора
Аутосомно-рецессивные мутации обнаруживают в гене LHCGR, что вызывает гипоплазию клеток Лейдига у мужчин. Генитальный фенотип варьирует от женского к мужскому, для которого типичен микропенис.
• Дефицит 5-альфа-редуктазы
5-альфа-редуктаза превращает тестостерон в более мощный DHT, который необходим для вирилизации мужских наружных половых органов. Гениталии у большинства детей с этим аутосомно-рецессивным состоянием, как правило, более неоднозначны, с различной степенью неполного лабиоскротального слияния и гипоспадии. Отличительной чертой биохимической аномалии является повышенное отношение Т к ДГТ (обычно> 30:1) после стимуляции ХГЧ в препубертатном периоде. Эти люди также проходят глубокую вирилизацию в период полового созревания.
• Синдром частичной андрогенной нечувствительности
Синдром вызывает дефект рецептора андрогенов. Изолированный микропенис обычно не является его проявлением, потому что гениталии обычно более неоднозначны. В этом состоянии уровень гонадотропинов и Т повышен. Поскольку ген, который кодирует андрогенный рецептор, расположен на Х-хромосоме, патология наследуется по Х-сцепленной схеме.
• Наиболее распространенные генетические синдромы
Синдром Клайнфелтера (47, XXY)
Особенности этого синдрома включают гипергонадотропный гипогонадизм, высокий рост, гинекомастию, уменьшение и уплотнение яичек, непропорционально длинные конечности, потенциальные трудности с обучением.
Синдром Прадера-Вилли
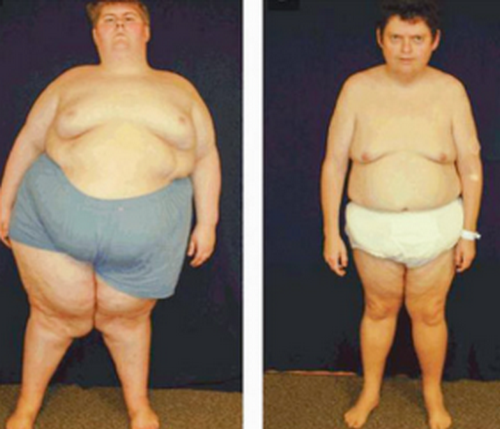
Гипогонадизм является особенностью синдрома Прадера-Вили и проявляется у мужчин крипторхизмом, недоразвитием мошонки, микропенисом. Характерные особенности болезни включают гипотонию, слабый сосательный рефлекс, отставание в физическом и психомоторном развитии в младенческом возрасте. У взрослых диагностируют ожирение из-за непреодолимого чувства голода, низкий рост, эмоциональную нестабильность и пр.
Синдром Бардета-Бидля
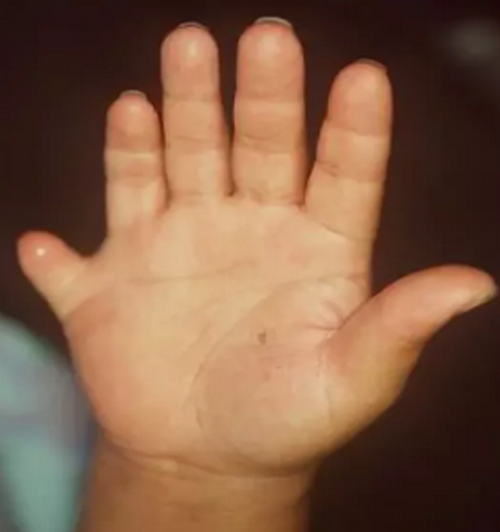
Особенности этого синдрома включают гипогонадотропный гипогонадизм, прогрессирующее нарушение зрения, ожирение, низкий рост, полидактилию, задержку развития, почечные аномалии, приводящие к терминальной стадии хронической почечной недостаточности, фиброз печени. Наследование этого синдрома имеет аутосомно-рецессивный характер, в нем участвуют мутации в 14 генах.
Синдром Нунана
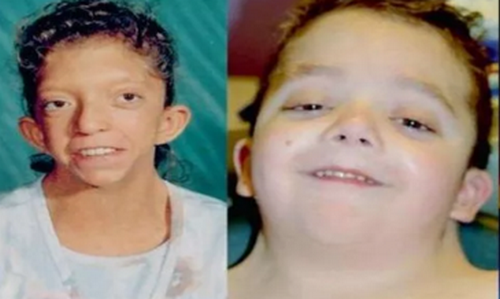
Особенности этого синдрома включают низкий рост, перепончатую шею, гипертелоризм, птоз, низкую заднюю линию роста волос, низко посаженные уши, деформации грудной клетки, крипторхизм, клапанный стеноз легочной артерии, лимфедему, нарушение работы свертывающей системы крови. Синдром Нунана наследуется по аутосомно-доминантному типу, примерно половина всех случаев представляет новые мутации. Изменения в гене PTPN11 обнаруживают в 50%, реже встречаются дефекты в KRAS, SOS1 и RAF1.
Диагностика микропениса
Младенца или ребенка с микропенисом следует тщательно обследовать на наличие дисморфных признаков и других врожденных аномалий, например расщелины губы и неба и других признаков гипоплазии лица. Аномальная скорость роста после первых 6-12 месяцев жизни предполагает дефицит гормона роста /и других гипофизарных гормонов. Важное значение имеет тщательное обследование половых органов, включая правильные измерения длины растянутого полового члена, положения отверстия уретры, а также расположения и размеров яичек. Одно или оба яичка могут отсутствовать в мошонке из-за недостатка тестостерона.
Лабораторная диагностика микропениса
План диагностических мероприятий вариативен и рассматривается в каждом случае индивидуально:
• Сделать кариотипирование рекомендуется для подтверждения хромосомного пола.
• Гонадотропины (ЛГ и ФСГ) достигают пубертатного уровня в возрасте 1-3 месяцев и снижаются примерно к полугоду. Чрезмерно высокие или низкие значения во время периода «минипубертатности» помогают сузить дифференциальный диагноз.
• Антимюллеровский гормон и ингибин B являются маркерами сохранности функций клеток Сертоли и могут быть полезны в качестве индикаторов присутствия тестикулярной ткани в условиях двустороннего крипторхизма.
• Уровни тестостерона и дигидротестостерона до и после стимуляции ХГЧ необходимы для оценки ответа яичек на введение гонадотропинов и дефицит 5-альфа-редуктазы (на что указывает повышенное отношение тестостерона к дигидротестостерону).
• Учитывая возможность пангипопитуитаризма, всех мальчиков с микропенисом наблюдают на предмет гипогликемии и признаков других метаболических нарушений. Исследуют: глюкозу, инсулин, кортизол, гормон роста и другие гормоны гипофиза.
Инструментальная диагностика при микропенисе
В ситуациях генитальной двусмысленности часто помогает УЗИ органов малого таза. Наличие матки и яичников убедительно свидетельствует о женском поле. При подозрении на гипопитуитаризм необходимо сделать МРТ головного мозга, чтобы оценить области гипоталамуса и гипофиза.
Лечение микропениса
Если гипогонадизм диагностирован как самостоятельное заболевание или является одним из симптомов какого-либо патологического процесса, проводят постоянную заместительную терапию андрогенсодержащими препаратами (первичный и вторичный гипогонадизм), или назначают гонадотропины (вторичный гипогонадизм). Цель лечения – нивелирование клинических проявлений, восстановление вторичных половых признаков.
Тестостерон является основным андрогенным гормоном, преимущественно образующимся в интерстициальных (лейдиговых) клетках яичек. В тканях-мишенях он превращается в более активную форму (DHT) с помощью 5-альфа-редуктазы и контролирует развитие и функционирование мужских половых органов и вторичные половые признаки. Он также вызывает системные анаболические эффекты, включая увеличение синтеза эритропоэтина, белка и накопление кальция в костной ткани. В младенческом возрасте при микропенисе, вне зависимости от причины, проводят терапию тестостероном по укороченным схемам, что рассматривается также в качестве этапа диагностики при хорошем ответе. Дигидротестостерон может применяться трансдермально, на кожу мошонки.
Назначение пролонгированных форм эфиров тестостерона при его подтвержденном дефиците используют для увеличения размера полового члена у мальчиков с 13-15 лет, более раннее лечение нерационально и способствует осложнениям. Многие дети с микропенисом, особенно на фоне дефицита гонадотропина, не имеют спонтанного или полного полового созревания. В этих случаях тестостерон используют для начала наступления пубертатного периода. Дозировка постепенно увеличивается до замещающей дозы у взрослых, имитируя естественное половое созревание. Некоторые пациенты вынуждены получать пожизненную заместительную терапию, но тестостерон не оказывает влияния на увеличение пениса после завершения полового созревания.
У пациентов с гипогонадотропным гипогонадизмом, которые желают сохранить фертильность, ХГЧ и рекомбинантный ФСГ могут быть назначены специалистом в области репродуктивной медицины для стимулирования секреции стероидов и сперматогенеза в соответствующее время.
Младенцы с другими гормональными нарушениями (дефицит гормона роста, гипотиреоз, надпочечниковая недостаточность) должны получать соответствующие препараты в качестве заместительной терапии.
Хирургические методы лечения микропениса

Если от лечения гормонами эффекта нет или их использование принято нецелесообразным, возможные варианты для решения проблемы:
• увеличение длины и толщины пениса, лигаментотомия и введение аутожира, синтетических препаратов и пр., если к пубертату удалось "подрастить" собственные ткани;
• фаллоуретропластика – полное формирование неофаллоса и мочеиспускательного канала.
Хирурги также выполняют операции для коррекции проблем с мочеиспусканием при эписпадии, гипоспадии. При крипторхизме производят низведение тестикул и их фиксацию в раннем детском возрасте, что позволяет избежать малигнизации и гипотрофии.
Прогноз при микропенисе
Прогноз у мальчиков с микропенисом, вторичным по отношению к дефициту тестостерона или гонадотропинов, обычно удовлетворительный. Пациенты хорошо реагируют на терапию тестостероном, что позволяет увеличить микропенис и сохранить сексуальную, и значительно реже – репродуктивную функцию. Прогноз гораздо более осторожен у детей с нечувствительностью к андрогенам, особенно с выраженной неопределенностью гениталий.
Автор
Виктория Мишина
Дата публикации




комментарии