Причины мужского бесплодия
Содержание статьи:
В последние десятилетия мужское бесплодие стало серьезной медицинской и социальной проблемой. Неспособность к зачатию может быть связана с разными причинами, а патогенез таких нарушений, как правило, отличается особой сложностью. Поэтому диагностика и разработка эффективных методов лечения мужского бесплодия представляют для медиков очень непростую задачу. Прежде всего, неудовлетворительные результаты терапии обусловлены невозможностью выявить точную причину бесплодия у мужчин.
Бесплодная пара
В современной медицинской практике семейную пару принято считать бесплодной, если зачатие не произошло после 12 месяцев регулярной интимной близости без применения контрацептивов. (Этот критерий был предложен ВОЗ в 2000 году).
В разных странах статистика бесплодия существенно различается. В целом в течение года зачатие не происходит у 10-25% супружеских пар. За врачебной помощью обращаются далеко не все из них – примерно от 15 до 50%. У каждой четвертой пары беременность наступает без лечения в двухлетний период. Каждой десятой паре удается зачать ребенка на протяжении четырехлетнего периода наблюдения. Для 2-10% семей зачатие невозможно. От 10 до 25% пар не могут иметь второго ребенка. И примерно 5% семей будут бездетными.
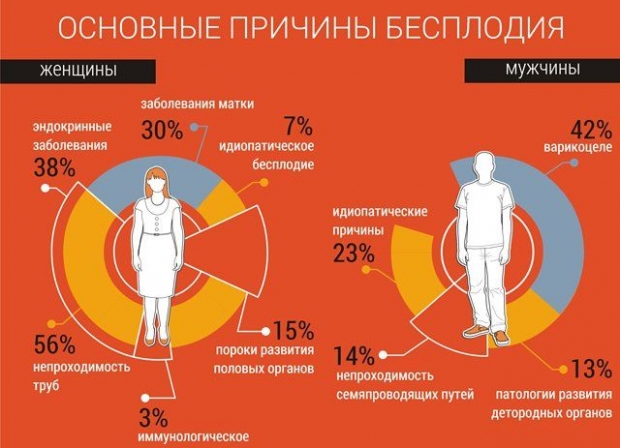
Мужское бесплодие
Можно утверждать, что рост числа случаев мужского бесплодия связан с неблагоприятным воздействием внешней среды, распространенностью болезней половой сферы, слишком высокой аллергизацией, врожденными патологиями органов половой сферы, неправильным употреблением медицинских препаратов, нездоровым образом жизни, вредными привычками.
Существует много факторов, которые могут привести к аномалиям в развитии сперматозоидов. Их делят на две группы – главные (то есть те, которые встречаются чаще всего) и дополнительные (они могут играть самостоятельную роль или же оказывать негативное воздействие в сочетании с основными причинами).
Основные причины мужского бесплодия
Основными причинами бесплодия у мужчин считаются:
- Болезни мочеполовой системы, имеющие инфекционно-воспалительную природу.
- Врожденные патологии, такие как эписпадия, гипоспадия, крипторхизм.
- Варикоцеле.
- Изолированные патологии семенной жидкости.
- Причины иммунологического характера.
- Патозооспермия невыясненного происхождения.
- Перенесенные в прошлом операции (связанные с паховой грыжей, гидроцеле, патологиями мочевого пузыря, стриктурой уретры).
- Некоторые виды консервативного лечения, такие как облучение, гормональная терапия, химиотерапия, транквилизаторы, сульфаниламиды, препараты от гипертонии, нитрофурановые производные.
- Прием некоторых наркотических веществ.
- Эндокринные факторы (гипогонадизм вторичный и первичный, тестостерондефицитные состояния, гиперпролактинемия).
- Эякуляторные и сексуальные проблемы.
Другие заболевания (почечная недостаточность, диабет, осложненный орхитом эпидемический паротит, хронические болезни органов дыхания, туберкулез, цирроз печени и некоторые другие).
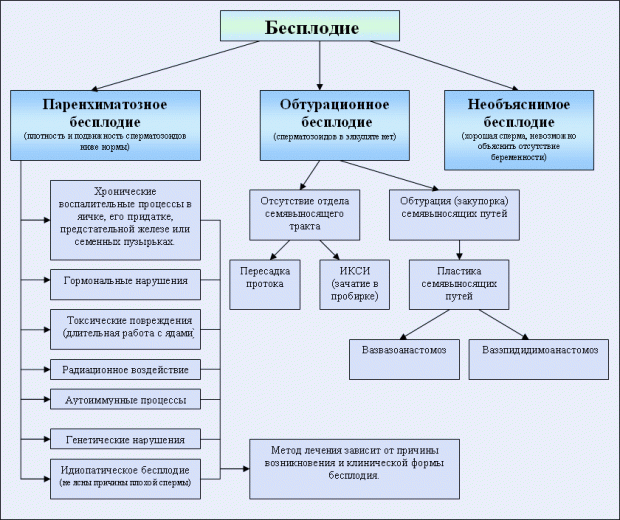
Факторы развития бесплодия у мужчин
К дополнительным причинам бесплодия у мужчин относятся:
- Работа в условиях воздействия пониженных или повышенных температур.
- Контакт с рядом неорганических и органических соединений.
- Эректильная дисфункция.
- Курение.
- Регулярное употребление спиртных напитков.
- Длительный подъем температуры тела более 38 градусов.
- Неправильный рацион.
- Травмы половых органов.
- Ссоры в семье и другие психологические причины.
Поскольку бесплодие может быть вызвано множеством различных причин, а его клинические проявления довольно разнообразны, возникают затруднения с терминологией и классификацией.
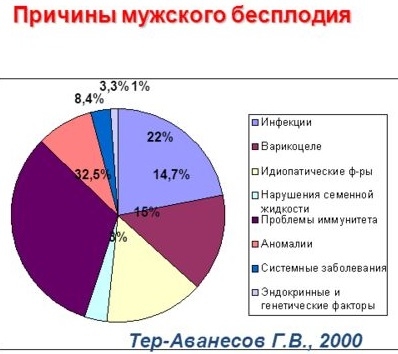
Иммунологическое бесплодие у мужчин
Почему развивается иммунологическое бесплодие
В зависимости от популяции распространенность иммунологического бесплодия колеблется в пределах от 5 до 15%. В подобных случаях невозможность полноценного развития мужских половых клеток и нарушение образования здоровой спермы обусловлены присутствием особых антител, которые атакуют сперматозоиды.
В последние годы начала интенсивно развиваться новая отрасль в иммунологии, которая получила название «иммунология репродукции». В рамках этого медицинского направления разрабатываются новейшие диагностические методики, помогающие выявить нарушения мужской репродуктивной функции на клеточном и даже молекулярном уровнях. Самым легко доступным является МАР-тест, который выполняют совместно со спермограммой.
Виды антител к сперматозоидам
Расскажем более подробно об антиспермальных антителах. Они представляют собой иммуноглобулины А, М и G, которые производятся в организме под влиянием изменений в иммунной регуляции.
Эти антитела различаются по принципу своего действия. Так, выделяют три типа антиспермальных антител:
• спермоиммобилизующие. Они обладают способностью обездвиживать мужские половые клетки;
• спермоагглютинирующие. Склеивают сперматозоиды;
• спермолизирующие – растворяющие.
Антиспермальные антитела обнаруживаются в сперме мужчины и в цервикальном канале его партнерши. Также могут выявляться в крови у партнеров или у одного из них.
Методика НИФ (непрямая иммунофлуоресценция) дает возможность обнаружить антитела и оценить их расположение на поверхности мужских половых клеток. Чаще всего антитела прикрепляются к телу сперматозоида, особенно к хвостовому отделу. В результате мужские половые клетки обездвиживаются. При закреплении антител на головке подвижность клеток не нарушается, но затрудняется попадание сперматозоида в яйцеклетку.
Нарушения могут быть нескольких видов. Их тип связан с количеством антител, местом их обнаружения, классом иммуноглобулинов. Так, в современной медицине выделяют:
- Проблемы с транспортом мужских клеток по женским половым путям.
- Невозможность полноценного развития сперматозоидов (вплоть до некрозооспермии).
- Невозможность оплодотворения яйцеклетки.
- Нарушение процесса имплантации эмбриона в матку.
Причины формирования антиспермальных антител в мужском организме
В половых железах мужчины сперматозоиды возникают лишь тогда, когда иммунная система распознает все ткани организма как свои, то есть становится толерантной к ним. Яички мужчины имеют особый барьер, которые не дает сперматозоидам контактировать с иммунными клетками. В случае нарушения этого барьера развиваются определенные иммунные реакции. К факторам, ведущим к повреждению защитного барьера, относят:
- Перенесенные операции или травмы.
- Проблемы с кровообращением в области половых органов (например при варикоцеле).
Ряд вирусных заболеваний (прежде всего, эпидемический паротит, который чаще называют «свинка»).
- Температурное воздействие (слишком высокие или слишком низкие температуры).
- Воспалительные процессы в яичках, придатках, семенных пузырьках, острый и хронический простатит.
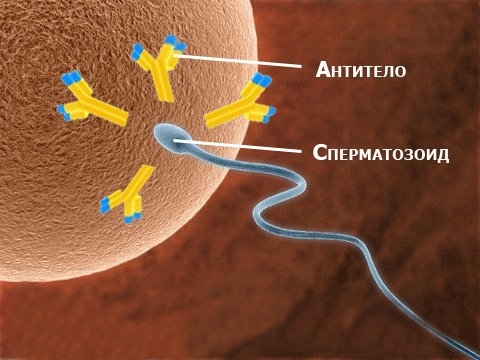
Где чаще находят антитела к сперматозоидам
По данным разных исследователей антиспермальные тела у бесплодных пар выявляются с такой частотой: у женщин – 32%, у мужчин - около 15 %. Экспериментальным путем и на практике подтверждается, что антитела к сперматозоидам чаще обнаруживаются в шеечной слизи и в сперме. Поэтому для проведения анализов на выявление антиспермальных антител больше всего подходят именно эти биологические материалы.
Важно помнить, чтобы выявление у одного партнера (или даже у обоих) антител к сперматозоидом вовсе не значит, что зачатие невозможно. Присутствие антиспермальных антител уменьшает вероятность беременности, но ни в коем случае не исключает ее полностью.
Иммунная реакция на сперматозоиды в женском организме
На данный момент особенности реакции женского иммунитета на сперматозоиды партнера изучены недостаточно. Женская половая система имеет возможность многократного контактирования со сперматозоидами мужчин, которые обладают чужеродными антигенами. У женщин с большим количеством половых партнеров происходит контакт с различными антигенами разных мужских половых клеток. То есть происходит постоянное иммунологическое стимулирование. Это создает условия для формирования иммунных реакций (системных и местных), в результате которых в женском организме формируются антиспермальные антитела.
Поддержанию данного иммунного механизма во многом способствуют и различные воспалительные процессы в половых органах женщины (прежде всего, хронические, например, воспаление придатков). Также имеют значение эндометриоз, повышенная аллергизация организма и ряд других факторов.
В ряде научных работ отмечается возникновение большого числа антител к сперматозоидам у бесплодных женщин, которые ранее подвергались процедуре введения в половые пути донорской спермы или спермы мужа. Причем выявлялись антиспермальные антитела в подобных случаях и в шеечной слизи, и в сыворотке крови.
Интересно отметить такой факт: чем больше процедур по введению спермы перенесла женщина, тем выше в ее организме число антител к мужским половым клеткам. Эту реакцию иммунитета можно объяснить тем, что сперматозоиды, введенные в женский организм искусственным способом, не находятся в семенном секрете и не имеют своего природного биологического окружения. Как известно, семенной секрет имеет в своем составе особые соединения – иммуноподавляющие факторы. Эти вещества обладают способностью подавлять иммунные реакции в женских половых путях. Благодаря этому антитела к сперматозоидам не синтезируются, и становится возможным оплодотворение яйцеклетки.
Нередко в женской половой системе возникают и местные реакции. Типичная локализация таких иммунных реакций - это шейка маки. Также возможно вовлечение в реакции маточных труб и эндометрия, иногда – влагалища.
Почему в женских половых путях возникает иммунная реакция на мужские половые клетки
Причину этого явления объясняют так. Слизистая шеечного канала содержит значительное число плазматических клеток - плазмацитов. Эти клетки обладают способностью производить некоторые составляющие иммуноглобулинов А. Кроме иммуноглобулинов А в шеечной слизи выявляют и другие классы иммуноглобулинов, которые принимают участие в местных иммунных реакциях, к примеру, иммуноглобулин класса G.
В разных работах отмечается связь между количеством в мужском организме этих антител и уменьшением подвижности половых клеток, их склеиванием и невозможностью проникнуть через слизистую пробку цервикального канала. Но все же стоит отметить, что далеко не всегда присутствие в крови антиспермальных антител влияет на фертильные способности мужчины. Дело в том, что антитела могут отсутствовать в половых путях. Или же на них оказывают влияние факторы, подавляющие иммунитет (такие факторы выявляются в шеечной слизи и в секрете семенных пузырьков).
То есть, можно утверждать, что иммунный эффект против сперматозоидов является следствием нарушений в работе естественных защитных механизмов человеческого организма.
В систему естественной защиты органов половой сферы входят такие элементы:
- Защитный барьер яичек.
- Способность семенной жидкости подавлять иммунитет.
- Иммунные регуляторные механизмы.
Генетическое бесплодие у мужчин
Поскольку в сперматогенезе участвует значительное число предполагаемых генов, можно сделать вывод, что идиопатические нарушения сперматогенеза в большинстве своем связаны с полиморфизмом или же мутациями генов-кандидатов. По этой причине проводились активные исследования, направленные на поиск новых маркеров. Однако никаких полиморфизмов и мутаций, имеющих клиническую значимость, выявлено не было (за исключением связанных с Y-хромосомой). По всей вероятности, существенного прогресса в этой сфере можно добиться, применяя новые аналитические подходы.
Почти в половине случаев мужское бесплодие бывает обусловлено отклонением от нормы показателей эякулята. Причем эти нарушения могут быть как качественными, так и количественными. Более чем в 30% случаев точную причину бесплодия выявить получается. Тогда считают, что оно связано с воздействием иммунологических или же генетических факторов.
Сперматогенез является сложным процессом, который состоит из многих этапов. Итогом этого процесса является формирование зрелых сперматозоидов. Если в генах, которые контролируют процесс образования мужских половых клеток, происходят мутации, то сперматозоиды теряют подвижность, нарушаются их морфологические характеристики, и они лишаются фертильной способности.
К примеру, в 10-15% случаев астенозооспермии выявляются микроделеции локуса AZF (Azoospermia Factor) Y-хромосомы. Эти же изменения обнаруживаются в 5-10% случаев тяжелой олигозооспермии выявленной при расшифровке анализа спермограммы.
Семейство DAZ (Deleted in Azoospermia) объединяет несколько разных генов, которые находятся в AZFс-субрегионе. В работе Ghorbel M. и коллег проанализированы ассоциации делеций DAZ2 и DAZ4 с неспособностью мужчины к зачатию. У пациентов с отсутствием всех четырех генов показатели спермограммы хуже, чем у мужчин, у которых сохранены два DAZ гена.
Существуют и другие генетические факторы, сильно затрудняющие лечение мужского бесплодия. Так, неэффективность терапии может быть обусловлена мутациями генов, ответственных за метаболизм лекарственных веществ.
Также имеют определенное значение и средовые факторы – действие физических и химических агентов, связанное с антропогенным влиянием на окружающую среду. Эти негативные внешние воздействия способствуют уменьшению фертильности спермы, снижая ее количественные показатели. К тому же внешние факторы могут привести к мутациям и повреждениям ДНК мужских половых клеток, что самым отрицательным образом сказывается на их морфологии и двигательной активности.
В последние десятилетия 20-го века начала вызывать особый интерес гипотеза, связанная с действием эндокринных дизрапторов. И сейчас она остается одной из наиболее популярных.
Эндокринные дизрапторы – это вещества, обладающие способностью к специфическому соединению с клеточными гормональными рецепторами. В результате таких сигналов возникают гормоноподобные эффекты.
Одним из наиболее распространенных эндокринных дизрапторов является дихлордифенилтрихлорэтан, а также его метаболиты. Они обладают способностью влиять на производство половых гормонов. Дикосины являются очень токсичными веществами и сильно загрязняют окружающую среду. Под их влиянием может замедлиться процесс полового созревания, и в итоге возникнет бесплодие (это актуально и для мужчин, и для женщин).
В материалах из пластмасс содержится бисфенол А. Даже небольшие дозы этого вещества способны ускорить половое созревание и нарушить сперматогенез.
Различные по своему происхождению синдромы гиперандрогенности в последние годы регистрируются все чаще. Этот факт принято объяснять социально-экономическими причинами, с которыми могут быть связаны нарушения в нейроэндокринном контроле работы желез.
К тому же, общеизвестно, что экспрессия многих генетических заболеваний происходит под влиянием самых разных негативных факторов: неправильно подобранная медикаментозная терапия, повышенный инфекционный индекс, неблагоприятные внешние воздействия и другое.
Микросомальная система метаболизма (другое название – система цитохрома Р-450) отвечает за реализацию двух крайне важных функций:
• участие в процессах эндогенного метаболизма;
• участие в начальной фазе биотрансформации ксенобиотиков, которые поступают извне (формирование функциональных гидрофильных групп).
Идиопатическое мужское бесплодие подтвердилось в результате обследования пациентов, организм которых подвергался воздействию курения, а также ряда эндокринных дизрапторов (трихлорфенол и октилфенол).
Также проводились исследования активности ферментов, относящихся к глутатион-S-трансферазам, которые метаболизируют множество ксенобиотиков. Устойчивость клеток к свободным радикалам и перекисному окислению липидов возможна благодаря процессу глутатионопосредованной детоксикации. Актуальными являются исследования, направленные на изучение связей между бесплодием мужчин и разными полиморфными вариантами генов GST. Так в работах зарубежных ученых отмечается повышение вероятности бесплодия у мужчин, имеющих нулевой генотип GSTT1 или GSTM1. Если же имеет место сочетание обеих делеций, то риск бесплодия у пациента становится очень высоким.
Вторая фаза метаболизма ксенобиотиков (детоксикация посредством ацетилирования) проходит с участием N-ацетилтрансфераз 2. Для Nat2 субстратами являются гидрозины, амины. Среди них много канцерогенов и ряд медикаментозных средств. При этом выполненные исследования не дают оснований установить зависимость между полиморфизмом Nat2 и идиопатическим нарушением репродуктивной функции у мужчин.
При помощи энзима каталазы разрушается пероксид водорода, который образуется в результате процессов окисления и является токсичным для организма веществом. Было обнаружено, что у пациентов, страдающих идиопатическим бесплодием, протективно значимым является генотип TT гена CAT.
Множество дискуссий вызвало присутствие генов на Х-хромосоме, которые отвечают за процесс формирования сперматозоидов. Выявленный на этой хромосоме ген влияет на гемотестикулярный барьер и на процесс развития клеток Сертоли. Функциональный анализ этого гена, проведенный несколько позже, подтвердил, что он играет определенную роль в активации андрогенных рецепторов при бесплодии у мужчин. Другие исследователи утверждают, что в основе нарушения мужской фертильности может лежать мутация гена убиквитинспецифичной протеазы 26.
На данный момент исследователям удалось выявить ассоциации полиморфных вариантов AR с клиническими параметрами при том или ином медицинском состоянии, которое связано с гипоандрогенией. При помощи гена AR кодируется белок, являющийся андрогеновым рецептором. AR имеет повторы 3 нуклеотидов CAG. Причем число этих повторов существенно различается – 8 – 25. Довольно часто мужская инфертильность бывает связана с проблемами в гормональной регуляции развития сперматозоидов. Главная роль в этом процессе отводится андрогенам. Половые гормоны путем взаимодействия со специфическими рецепторами предопределяют формирование половых признаков мужчины, запускают процесс сперматогенеза и способствуют его поддержанию. Ряд авторов отмечает, что при меньшем количестве повторов конформационные изменения в рецепторе выражены меньше, а связь «гормон-рецетор» делается более прочной. Благодаря этому возрастает транскрипционная активность АР. Чем больше повторов CAG, тем слабее становится связь «гормон-рецептор». При этом транскрипционная активность AР уменьшается, снижается чувствительность к тестостерону, что связано с повышенным риском возникновения олигозооспермии. При падении уровня андрогенов производство спермы также сильно ухудшается. Мужчины, имеющие более 32 повторов, страдают очень тяжелыми нарушениями сперматогенеза.
Было проведено исследование с участием двух групп пациентов. Первая группа состояла из мужчин, страдающих азооспермией, а во вторую группу входили пациенты с олигозооспермией. В результате выяснилось, что в первой группе частота аллелей с короткими повторами CAG (от 18) была выше. Что касается второй группы, то здесь выше была частота аллелей с длинными повторами – от 28. Таким образом, можно предполагать, что между числом повторов и нарушением процесса образования мужских половых клеток существует связь.
По результатам работы других исследователей также выяснилось, что транскрипционная активность AR уменьшается, когда растет длина повторов CAG. Кроме того, был проанализирован CAG-полиморфизм рецептора андрогенов у пациентов, имеющих идиопатическую инфертильность. Такие изменения можно считать маркером предрасположенности к фертильным нарушениям.
К перспективным направлениям исследований можно отнести исследование влияния генов репарации ДНК на формирование чувствительности генома к воздействию негативных внешних факторов. PARP-1 принимает участие в ремоделировании хроматина. Ученым удалось выяснить, что генотип PARP1*CC(rs1136410) часто отмечается у пациентов, страдающих олигоспермией.
Фолиевая кислота необходима для синтеза ДНК. При работе с пациентами, репродуктивная функция которых понижена, был проведен анализ связи полиморфизмов MTHFR(C677T, A1298C), MTRR(A66G) с нарушениями мейоза. Связь между нарушением фолатного обмена и хромосомными аномалиями в сперматозоидах была подтверждена.
Почему возникает бесплодие у мужчин
Необходимо всегда учитывать тот факт, что инфертильность мужчин – это патология, связанная с действием множества факторов. Эта многофакторность существенно затрудняет диагностику мужского бесплодия. Ведь для каждого пациента необходимо тщательно проанализировать все возможные причины, какие-то из них исключить, выявить главную проблему. Ситуация может стать еще более сложной, если невозможность зачать ребенка связана с присутствием определенных факторов у обоих партнеров.
Подводя итоги, перечислим основные причины мужской инфертильности:
- Варикоцеле.
- Половые инфекции.
- Астенозооспермия.
- Олигозооспермия.
- Тератозооспермия.
Причем у каждого третьего мужчины с бесплодием действуют два и более из этих факторов. У некоторых пациентов причина инфертильности остается неизвестной.
Итак, изложенные выше факты подтверждают необходимость генетических исследований при диагностике мужской инфертильности. Информация, полученная из научной литературы, дает возможность больше узнать о причинах фертильных нарушений и позволяет уменьшить количество случаев идиопатического мужского бесплодия.
Выявление ассоциаций полиморфных вариантов генов с бесплодием у мужчин имеет два крайне важных аспекта. Прежде всего, многие исследования являются недостаточными из-за слишком маленького объема выборки, фенотипической и этнической разнородности. К тому же изучать полиморфизм одного гена в контексте нарушений фертильности нет смысла.
Благодаря огромному прогрессу в сфере молекулярно-генетических технологий появляются возможности для новых перспективных исследований, которые помогут составить четкое представление о генетической архитектуре мужской инфертильности.





комментарии
2018-11-21 04:59:25
Пашаспасибо
2018-10-22 12:23:06
питспс
2018-10-21 17:32:24
ВячеславА у нас вот был мужской фактор бесплодия, спермограмма была плохенькая. Хорошо, что врач подобрал грамотное лечение (муж принимал эффекс трибулус и на курсы физиотерапии ходил) В итоге это дало свои результаты, сейчас уже дочку ждем)
2018-05-25 10:54:39
мипинтересно